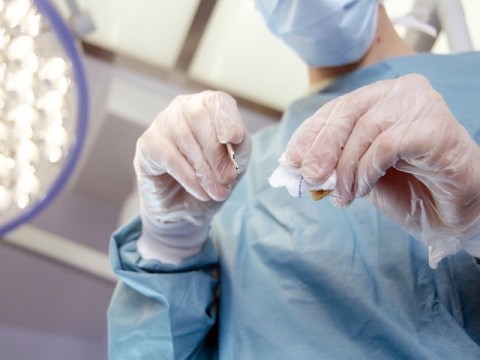
再生医療で細胞提供が可能な人が60% 大病した経験の有無が抵抗感に影響
2017年03月23日 06:20
日本の再生医療製品や遺伝子治療製品などの新規医療技術製品においては、製品の品質・安全性等からヒトへの投与の妥当性を評価するための治験申請の前段階として、独立行政法人医薬品医療機器総合機構による審査が必要となるなど、諸外国の制度的枠組みと比較して厳格に進められている。
週末コラム、話題のニュースを斬る!
アクセスランキング
Copyright(C)2012-2026 Economic News 無断転載を禁じます。